티칭백과란?
교과별 특성을 고려한 맞춤형 콘텐츠로서, 스마트한 수업과 자기주도학습을 지원하는 온라인 백과사전 서비스입니다.
- 지원 서비스
- - 주제별 맞춤 지식 공유
- - 다양한 스마트 기기 지원
- - 멀티미디어 자료 제공
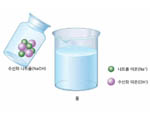
염기와 수산화 이온
염기는 물에 녹아 음이온인 수산화 이온(OH-)과 양이온으로 이온화되므로 수산화 이온(OH-)에 의해 염기의 공통성이 나타난다.
수산화 나트륨, 수산화 칼륨 등은 대표적인 염기성 물질이다. 이들은 물에 녹아 다음과 같이 이온화한다.
· 수산화 나트륨: NaOH → Na+ + OH-
· 수산화 칼륨: KOH → K+ + OH-
· 수산화 칼슘: Ca(OH)2 → Ca2+ + 2OH-
앞의 식을 보면 각 물질들이 공통적으로 하이드록시기(-OH)를 가지고 있으며, 물에 녹아서 수산화 이온(OH-)을 발생시키는 것을 볼 수 있다. 이와 같이 물에 녹아 수산화 이온을 만들어 내는 물질을 염기라고 하고, 염기가 녹아 있는 물질을 염기성 용액이라고 한다. 하지만 메탄올이나 에탄올의 경우 하이드록시기를 가지고 있어도 물에 녹아 수산화 이온을 만들지 못하므로 염기가 아니다.
· 메탄올: CH3-OH
· 에탄올: C2H5-OH
반대로 암모니아는 하이드록시기(-OH)가 없지만 물과 반응하여 수산화 이온(OH-)을 발생시키므로 염기에 속한다.
NH3 + H2O → NH4+ + OH-
암모니아 물 암모늄 이온 수산화 이온
- OX 문제염기는 물에 녹아 수산화 이온(OH-)과 양이온을 내놓는다.
참고자료
더보기 >관련용어
지식나눔
관련된 나의 지식을 등록하여 공유할 수 있습니다.
의견나눔
총 0개의 의견이 있습니다.